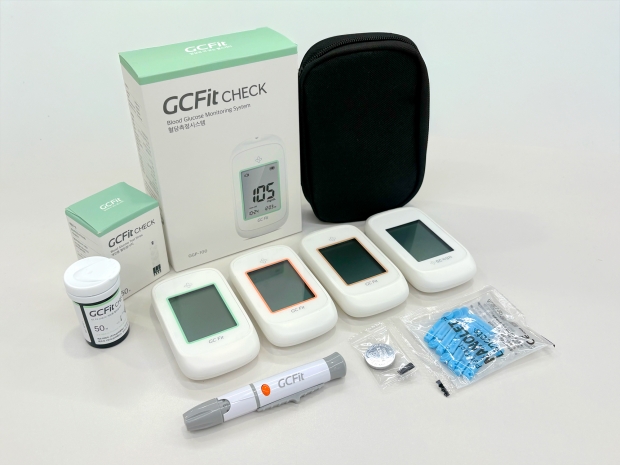
GC녹십자엠에스가 혈당측정시스템 ‘GC Fit(모델명 GGP-100)’으로 유럽 체외진단의료기기 규정(CE-IVDR) 인증을 획득하며 유럽 시장 진출을 본격화한다. 회사는 이번 인증을 통해 제품의 안전성과 성능을 공식적으로 인정받았으며, 출시 시점도 기존 계획보다 앞당겼다.
CE-IVDR(In Vitro Diagnostic Medical Device Regulation, 체외진단 의료기기 규정)은 유럽연합(EU)이 적용하는 체외진단기기 규제로, 기존 CE-IVDD 지침 대비 성능과 안전성 기준이 대폭 강화된 제도다. 2017년 제정 이후 전환 기간을 거쳐 현재 모든 EU 회원국에서 시행되고 있으며, 유럽 시장 진입을 위한 필수 요건으로 평가된다.
이번에 인증을 획득한 ‘GGP-100’은 비교적 높은 위험군에 해당하는 Class-C 제품으로 분류된다. GC녹십자엠에스는 해당 제품의 인증을 통해 기술적 신뢰성을 입증했으며, 기존 그립형 혈당측정기를 포함한 전체 혈당 측정 제품군이 유럽 기준을 충족하게 됐다고 설명했다.
회사 측은 이번 인증으로 유럽 시장 진입 시점을 기존 계획보다 약 2개월 앞당길 수 있게 됐다고 밝혔다. 아울러 광학 방식 헤모글로빈(Hb) 측정 제품 역시 CE-IVDR 인증을 확보해 향후 수출 확대 기반을 마련한다는 계획이다.
GC녹십자엠에스 관계자는 “이번 인증은 회사의 진단 기술이 유럽 규제 기준을 충족했음을 보여주는 결과”라며 “혈당 측정 시스템을 시작으로 다양한 진단 제품군을 확대해 유럽 시장 내 경쟁력을 강화해 나갈 것”이라고 밝혔다.
뉴스타운
뉴스타운TV 구독 및 시청료 후원하기
뉴스타운TV























![[단독] 북한산 인수봉, 구조 헬기 긴급 출동 장면 포착!](https://cdn.newstown.co.kr/news/photo/202511/669971_628773_447.jpg)






